降低抗炎药毒副作用(专业版)
非甾体类抗炎药(NSAIDs)是一大类具有解热(退烧)、镇痛、消炎性能的药物,市场上已有百余种上千个品牌。
英文名称:Non-steroidal Anti-inflammatory Drugs Poisoning,NSAIDs Side-effects
定义
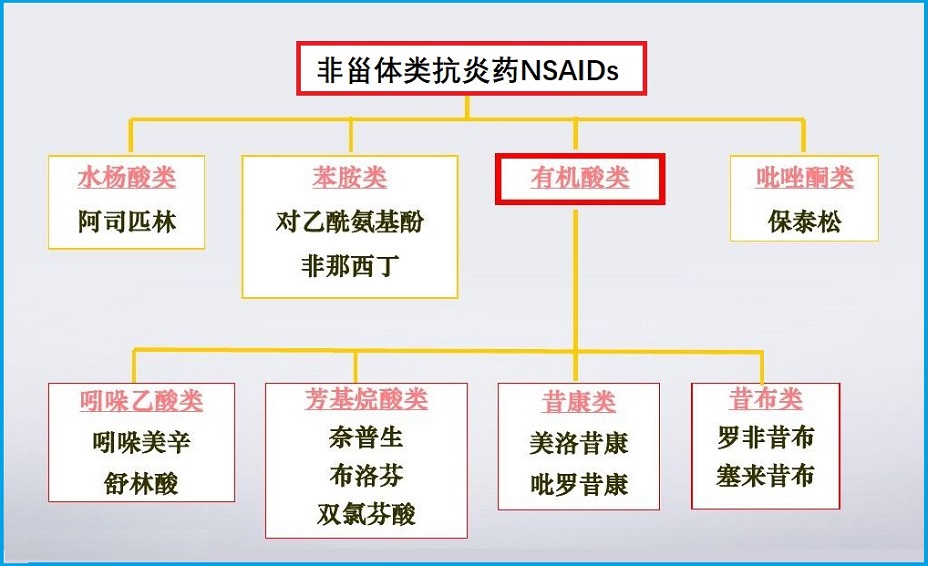
非甾体类抗炎药(NSAIDs)是一大类具有解热(退烧)、镇痛、消炎性能的药物,市场上已有百余种上千个品牌。长期服用非甾体类抗炎药,可能引起消化道溃疡和出血、心血管病和慢性肾损伤等不良反应。常见的非甾体类抗炎药包括如下:
- 乙酰水杨酸盐类,如阿司匹林。
- 非乙酰基水杨酸盐类,如水杨酸镁、水杨酸钠、水杨酸胆碱镁。
- 非水杨酸盐类,包括布洛芬、芬必得、吲哚美辛(消炎痛)、萘普生、氟比布洛芬、萘丁美酮(萘普酮)、苯氧基布洛芬、吡罗昔康(炎痛喜康)、保泰松、双氯灭痛等。
NSAIDs毒副作用机制和表现
NSAIDs药物通过抑制环氧化酶(COX)的活性,从而抑制花生四烯酸生成前列环素(PGI1)、前列腺素(PGE1,PGE2)和血栓素A2(TXA2)。其中,前列腺素有许多功能,包括抑制胃酸分泌、促进钠排泄,降低血压、使血管通透性增加、抑制血小板聚集,以及调节肾血流和促进骨吸…等。NSAIDs药物主要副作用表现在:
- 胃肠道:主要是COX-1抑制剂,如阿司匹林、布洛芬等,轻度症状如恶心、胃灼热和胃痛等,严重如胃、十二指肠溃疡、出血甚至胃穿孔等。
- 心血管毒性:主要是COX-2抑制剂,用于类风湿和骨关节炎等,如尼美舒利、美洛昔康、塞来昔布和罗非昔布等。可影响血管收缩、血栓形成、血管清除过量胆固醇等,以及刺激产生有害的炎性因子等。
- 肾脏毒性,长期服用NSAIDs,可导致肾脏灌注和肾小球滤过率下降,致使体液和电解质紊乱,引起肾脏功能不全、间质性肾炎及肾小管坏死等,对于年龄在60岁以上,以及慢性病患者如动脉硬化、高血压和肝退化等患者尤为明显。
- 线粒体障碍和自由基损伤:NSAIDs干扰细胞线粒体功能,可能产生更多的自由基。
影响NSAIDs的因素
可增加NSAIDs药物毒副作用的因素,包括如下:- 年龄:超过60岁的人更容易形成NSAIDs相关性溃疡,以及心血管病事件。
- 健康状况:胃肠道病史,肾、肝功能受损,糖尿病、类风湿关节炎和高血压等。
- 剂量和疗程:使用高剂量或多个非甾体类抗炎药,导致胃肠道并发症风险显著增加,而心血管病与非甾体类抗炎药的使用时间风险相关联。
- 药物种类:同时使用阿司匹林等NSAIDs药和糖皮质激素、抗凝药,血小板抑制剂和5-羟色胺再摄取抑制剂,可显著增加胃肠道溃疡或出血。
如何降低NSAIDs毒副作用
综合疗法包括如下:营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控抗炎药毒性营养和草本补充剂,主要包括如下:
经常服用对乙酰氨基酚和非甾体抗炎药的人应该意识到这些药物会引起肝脏和肾脏毒性。在服用这些药物时,最好提供抗氧化支持来保护这些器官。
一、降低肝损伤:
1.含硫氨基酸:
摄入对乙酰氨基酚后,含硫氨基酸有助于肝脏健康。对于那些长期服用对乙酰氨基酚(扑热息痛)或非甾体抗炎药(NSAIDs)的人来说,每天补充含硫氨基酸和其他化合物以支持谷胱甘肽水平,可以防止药物引起的毒性。
1.1.N-乙酰半胱氨酸(NAC):
高剂量NAC是对乙酰氨基酚过量的常规治疗药物。它也是治疗其他药物毒性引起的急性肝衰竭的有效方法1。任何时候服用对乙酰氨基酚时,都应同时服用至少600mg NAC,以帮助防止肝毒性。
1.2.甲硫氨酸(蛋氨酸):
甲硫氨酸是几种含硫抗氧化剂(包括半胱氨酸和谷胱甘肽)的必需氨基酸前体,充足的蛋氨酸是维持谷胱甘肽水平所必需的。蛋氨酸被用作对乙酰氨基酚过量的替代常规解药;尽管缺乏比较对照试验使得难以确定其在人类中对NAC的相对疗效2。在世界一些地区,甲硫氨酸(10%)被包含在对乙酰氨基酚产品中,以防止意外中毒;一项针对大鼠的单片组合研究表明,在对乙酰氨基酚的治疗剂量(100mg/kg)和高毒性剂量(1000mg/kg)下,包括甲硫氨酸可以最大限度地减少肝毒性(通过血清ALT和AST测量)3。
1.3.S-腺苷蛋氨酸(SAMe):
SAMe是一种甲硫氨酸衍生物,对核酸、蛋白质和磷脂(对乙酰氨基酚过量后恢复所需的化合物)的合成至关重要。对乙酰氨基酚可降低肝细胞细胞核和线粒体中的SAMe水平4。在一项研究中,当小鼠服用对乙酰氨基酚过量一小时内,SAMe和NAC的疗效(作为解药)相当5。
2.硒:
硒是合成谷胱甘肽和对乙酰氨基酚解毒酶的辅因子。在一个实验小鼠模型中,硒缺乏显著降低了对乙酰氨基酚致死剂量的大小6。在对乙酰氨基酚过量服用前24小时给大鼠注射硒,可显著防止肝毒性,降低ALT和AST(肝损伤标志物)水平,并增加肝谷胱甘肽水平7。口服硒(0.5mg/kg体重)与NAC(500mg/kg体重)联合给大鼠服用对乙酰氨基酚过量1小时内,显示出比单独给药NAC更大的保护作用8。
3.类胡萝卜素:
已经在大鼠模型中检测了几种类胡萝卜素对乙酰氨基酚过量的保护作用。过量服用前7天服用的叶黄素(50-250mg/kg/天)可保持谷胱甘肽水平,并降低对乙酰氨基酚的ALT和AST升高9。过量服用后连续7天给予富含番茄红素的番茄提取物(5mg/kg/天)具有类似的保护作用10。单剂量的β-胡萝卜素(30mg/kg)或玉米黄质(50-250mg/kg)与有毒的对乙酰氨基酚剂量同时服用可降低血清肝酶,在玉米黄质的情况下,可降低肝组织损伤的显微镜证据11,12。
4.水飞蓟:
水飞蓟素是水飞蓟中几种相关多酚化合物的混合物13,通过几种互补机制促进解毒。水飞蓟素的抗氧化能力可以降低与大鼠对乙酰氨基酚代谢相关的氧化应激(肝脏中),这具有保护细胞谷胱甘肽水平的作用14。和NAC一样,水飞蓟素可以防止对乙酰氨基酚的毒性。此外,一项动物研究表明,如果治疗延迟,它可能比NAC对乙酰氨基酚毒性更有效(在小鼠模型中,过量服用后24小时内有效)15。
5.姜黄素:
当在实验性对乙酰氨基酚中毒后30分钟内给大鼠服用时,与对照大鼠相比,200mg/kg姜黄素可防止肾损伤的微观表现,防止肾脂质过氧化升高,并保持谷胱甘肽水平16。大鼠口服50或100mg/kg/天预处理7天,显著降低实验性对乙酰氨基酚过量后的肝损伤标志物(ALT、AST和脂质过氧化)17。姜黄素还可以提高NAC作为对乙酰氨基酚解药的疗效;在200mg/kg NAC中添加25mg/kg姜黄素可保护大鼠肝脏和肾脏免受对乙酰氨基酚的毒性,其疗效相当于800mg/kg NAC18。
6.辅酶Q10(CoQ10):
在对乙酰氨基酚过量服用之前或之后,通过注射辅酶Q10治疗大鼠,可以保护大鼠免受肝脏损伤。静脉注射辅酶Q10(5mg/kg)预处理降低了血清ALT和氧化应激标志物,但对肝脏谷胱甘肽水平没有影响19。对乙酰氨基酚中毒后1小时和12小时两次注射辅酶Q10(每次10mg/kg),可显著降低ALT、AST和炎性细胞因子水平,抑制脂质过氧化,保存谷胱甘肽,减少组织死亡20。
7.维生素C:
与对乙酰氨基酚同时给予高剂量的抗坏血酸棕榈酸酯(相当于600mg/kg的游离维生素C)可以防止小鼠血清肝酶的升高,并降低对乙酰氨基苯酚介导的死亡率21。在小鼠模型中,游离维生素C(抗坏血酸)不能防止肝脏或肾脏损伤21,22。
8.褪黑素:
在对乙酰氨基酚过量服用前4或8小时用口服褪黑素(50或100mg/kg)治疗小鼠,以剂量和时间依赖的方式抑制血清ALT和AST活性的增加,但对肝脏谷胱甘肽水平没有影响。当在服药过量前4小时给予时,观察到肝坏死的显著抑制23。对乙酰氨基酚过量服用前注射褪黑素(10mg/kg)可能比“抢救”剂量更有效地降低肝毒性24,尽管相同剂量的抢救治疗已被证明能有效保护肾组织免受细胞死亡的影响25。
二、胃肠道支持:
非甾体抗炎药(NSAIDs)的一些胃肠道副作用可以利用胃保护营养素来解决,包括如下
1.肌肽锌:
肌肽锌(锌-肌肽螯合物)是一种胃保护剂,可以减少非甾体抗炎药诱导的胃肠道上皮细胞死亡,可能通过猝灭活性氧发挥作用26。锌肌肽是日本的一种处方抗溃疡药物,在日本已经研究和使用了几十年27,28。研究人员使用示踪剂化合物监测动物胃中的制备过程,观察到这种组合比单独使用锌或肌肽更有效地粘附在胃壁上,使这两种成分的有益效果都能传递到需要保护的部位29。
在2007年的一项人体试验中观察到了保护作用;10名服用肌肽锌(37.5mg,每日两次)的健康志愿者受到保护,免受吲哚美辛治疗引起的胃肠道通透性增加三倍的影响30。
2.甘草:
在欧洲历史上一直被用作胃保护/溃疡愈合剂31,32。非处方溃疡治疗药物甘珀酸(Carbenoxolone,或称生胃酮)是甘草中一种天然化合物的衍生物。甘草汤剂(以2.5g/kg体重给药)治愈了阿司匹林诱导的大鼠胃溃疡。愈合效果与两种处方治疗(质子泵抑制剂奥美拉唑和合成前列腺素米索前列醇)相似,但在预防方面(溃疡发生前)无效33。
在另一项动物研究中,与单独使用任何一种物质相比,解甘草甜素(DGL)与反流药物西咪替丁联合使用对阿司匹林诱导的粘膜损伤提供了更大的保护34。与全甘草不同,DGL提取物在不含甘草酸(全甘草的一种成分,已被证明会引起高血压等副作用)的情况下提供胃保护作用34,35。
3.乳香(提取物):
从乳香植物中提取的乳香酸本身就是抗炎化合物;它们抑制促炎酶5-脂氧合酶(5-LOX)的活性,并在炎症疾病(包括哮喘、骨关节炎和克罗恩病)的动物和人类模型中显示出改善作用36。乳香酸也可以预防NSAIDs诱导的胃溃疡;在一项研究中,用口服乳香提取物(250mg/kg)预处理的大鼠表现出比对照动物明显更少的阿司匹林或吲哚美辛诱导的胃溃疡(通过定性测定确定)37。
更多内容可点击其个性化综合干预方案如下:
以及参阅如下专文了解更多有关内容:
医疗干预
为减少或治疗NSAIDs药物引起消化道溃疡,一般考虑与胃保护剂的联合治疗,包括:
- H2受体拮抗剂,如西咪替丁、雷尼替丁和法莫替丁等。
- 质子泵抑制剂,如奥美拉唑、兰索拉唑和埃索美拉唑等。
预防
一些措施可以减少或避免抗炎药毒副作用,包括如下:- 限制服用药物:只有在绝对必要时才服用非处方药或处方药。·
- 仅按照指示服用药物。
- 服药期间禁止饮酒,尤其在服用止痛药时。
- 避免让儿童接触药物和化学品,包括维生素、草药补充剂等。
参考文献:
1. Ghabril M, Chalasani N, Björnsson E. Drug-induced liver injury: a clinical update. Curr Opin Gastroenterol. 2010;26(3):222–6.
2. Buckley N and Eddleston M. Paracetamol (acetaminophen) poisoning. ClinEvid (Online).2007;(14):1738–44.
3. Iyanda A et al. Effect of methionine on hepatic indices in male Wistar rat dosed to acetaminophen formulation. African Journal of Pharmacy and Pharmacology. 2010;4(9):653–7.
4. Brown JM et al. Temporal study of acetaminophen (APAP) and S-adenosyl-L-methionine (SAMe) effects on subcellular hepatic SAMe levels and methionine adenosyltransferase (MAT) expression and activity. ToxicolApplPharmacol. 2010;247(1):1–9.
5. Terneus MV et al. Comparison of S-adenosyl-L-methionine (SAMe) and N-acetylcysteine (NAC) protective effects on hepatic damage when administered after acetaminophen overdose. Toxicology. 2008;244(1):25–34.
6. Peterson FJ et al. Potentiation of acute acetaminophen lethality by selenium and vitamin E deficiency in mice. J Nutr. 1992;122(1):74–81.
7. Schnell RC et al. Protective effects of selenium on acetaminophen-induced hepatotoxicity in the rat.Toxicol Appl Pharmacol. 1988;95(1):1–11.
8. Yalçin S et al. Synergistic action of sodium selenite and N-acetylcysteine in acetaminophen-induced liver damage. Hum Exp Toxicol. 2008;27(5):425–9.
9. Sindhu ER et al. Carotenoid lutein protects rats from paracetamol-, carbon tetrachloride- and ethanol-induced hepatic damage. J Pharm Pharmacol. 2010;62(8):1054–60.
10. Jamshidzadeh A et al. Effects of tomato extract on oxidative stress induced toxicity in different organs of rats. Food ChemToxicol. 2008;46(12):3612–5.
11. Zahra T et al. Effects of Beta Carotene on Liver Enzymes in Acetaminophen Treated Rats. Journal of Rawalpindi Medical College (JRMC). 2010;14(1):7–10.
12. Firdous AP et al. Hepato-protective potential of carotenoid meso-zeaxanthin against paracetamol, CCl4 and ethanol induced toxicity. Indian J Exp Biol. 2011;49(1):44–9.
13. Abenavoli L et al. Milk thistle in liver diseases: past, present, future. Phytother Res. 2010;24(10):1423–32.
14. Campos R et al. Silybindihemisuccinate protects against glutathione depletion and lipid peroxidation induced by acetaminophen on rat liver. Planta Med. 1989;55(5):417–9.
15. Hau DKP et al. Novel use of silymarin as delayed therapy for acetaminophen-induced acute hepatic injury. Forsch Komplementmed. 2010;17(4):209–13.
16. Cekmen M et al. Curcumin prevents oxidative renal damage induced by acetaminophen in rats. Food ChemToxicol. 2009;47(7):1480–4.
17. Girish C et al. Hepatoprotective activity of picroliv, curcumin and ellagic acid compared to silymarin on paracetamol induced liver toxicity in mice. Fundam Clin Pharmacol. 2009;23(6):735–45.
18. Kheradpezhouh E et al. Curcumin protects rats against acetaminophen-induced hepatorenal damages and shows synergistic activity with N-acetyl cysteine. European Journal of Pharmacology. 2010;628(1-3):274–81.
19. Amimoto T et al. Acetaminophen-induced hepatic injury in mice: the role of lipid peroxidation and effects of pretreatment with coenzyme Q10 and alpha-tocopherol. Free Radic Biol Med. 1995;19(2):169–76.
20. Fouad AA et al. Hepatoprotective effect of coenzyme Q10 in rats with acetaminophen toxicity. Environ. Toxicol Pharmacol. 2012;33(2):158–67.
21. Jonker D et al. Comparison of the effects of ascorbylpalmitate and L-ascorbic acid on paracetamol-induced hepatotoxicity in the mouse. Toxicology. 1988;52(3):287–95.
22. Abraham P. Mega dose of vitamin C augments the nephrotoxicity of paracetamol. Nephrology (Carlton). 2005;10(6):623–4.
23. Matsura T et al. Mechanisms of protection by melatonin against acetaminophen-induced liver injury in mice. J Pineal Res. 2006;41(3):211–9.
24. Kanno SI et al. Melatonin protects on toxicity by acetaminophen but not on pharmacological effects in mice. Biol Pharm Bull. 2006;29(3):472–6.
25. Ilbey YO et al. Melatonin prevents acetaminophen-induced nephrotoxicity in rats. IntUrolNephrol. 2009;41(3):695–702.
26. Omatsu T et al. Reactive oxygen species-quenching and anti-apoptotic effect of polaprezinc on indomethacin-induced small intestinal epithelial cell injury. J Gastroenterol. 2010;45(7):692–702.
27. Matsukura T et al. Applicability of zinc complex of L-carnosine for medical use. 2000 Jul;65(7):817-23.
28. Cho CH et al. The membrane-stabilizing action of zinc carnosine (Z-103) in stress-induced gastric ulceration in rats. Life Sci. 1991;49(23):L189-94.
29. Furuta S et al. Residence time of polaprezinc (zinc L-carnosine complex) in the rat stomach and adhesiveness to ulcerous sites. 1995 Apr;67(4):271-8.
30. Mahmood A et al. Zinc carnosine, a health food supplement that stabilises small bowel integrity and stimulates gut repair processes. Gut. 2007;56(2):168–75.
31. Wittschier N et al. Aqueous extracts and polysaccharides from liquorice roots (Glycyrrhizaglabra L.) inhibit adhesion of Helicobacter pylori to human gastric mucosa. J Ethnopharmacol. 2009 Sep 7;125(2):218-23.
32. Aly AM et al. Licorice: a possible anti-inflammatory and anti-ulcer drug. AAPS PharmSciTech. 2005;6(1):E74–82.
33. Sancar M et al. Comparative effectiveness of Glycyrrhizaglabra vs. omeprazole and misoprostol for the treatment of aspirin-induced gastric ulcers. African Journal of Pharmacy and Pharmacology. 2009;3(12):615–20.
34. Bennett A et al. Aspirin-induced gastric mucosal damage in rats: cimetidine and deglycyrrhizinatedliquorice together give greater protection than low doses of either drug alone. 1980 Feb;32(2):151.
35. Das SK et al. Deglycyrrhizinatedliquorice in aphthous ulcers. 1989 Oct;37(10):647.
36. Anonymous. Boswellia serrata. Monograph. Altern Med Rev. 2008;13(2):165–7
37. Singh S et al. The gastric ulcer protective effect of boswellic acids, a leukotriene inhibitor from Boswelliaserrata, in rats. Phytomedicine. 2008;15(6-7):408–15
参考来源:
美国疾控中心有毒物质和疾病登记处
http://www.atsdr.cdc.gov
美国职业安全和卫生管理局
http://www.osha.gov
美国国立卫生研究院公众健康网
www.medlineplus.gov
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

